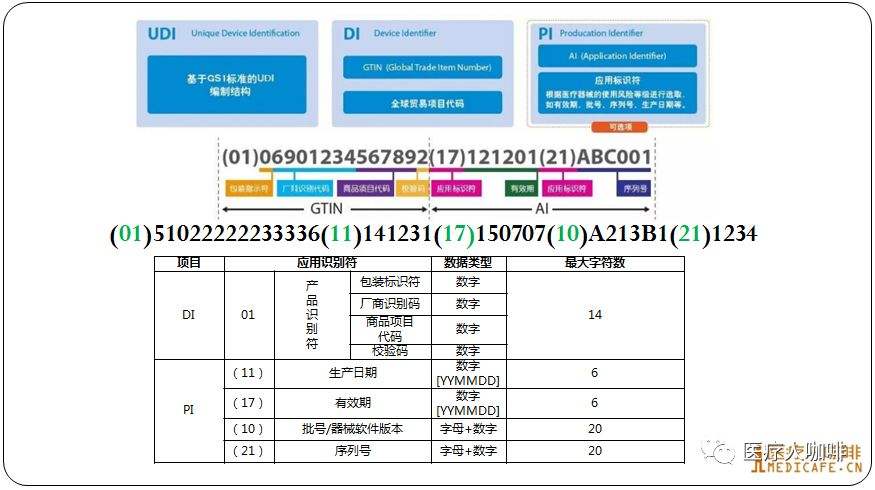
首先我们先回顾一下整个欧盟UDI实施的流程:
欧盟UDI实施的流程可以分为五步:
1、申请并获取厂商代码
2、编制UDI-DI
3、编制UDI-PI
4、制作UDI 一维、二维条码或RFID标签
5、EUDAMED UDI数据库申报
三、编制 UDI-PI
我们第三步是依据控制器械生产的方式,编制 UDI-PI。
UDI-PI 由企业根据自己的产品特性来编辑,我们来看一下GS1 的 PI 编码和范例图:

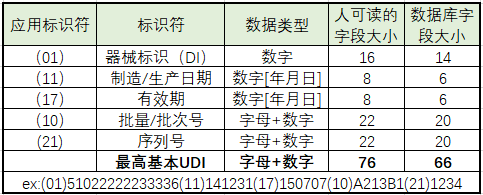
企业可以根据实际情况选择相关信息来编制PI。
举例:
A企业选择用生产日期+有效期 来编制PI,产品生产日期是2021-5-17.有效期是两年,那PI就是:(11)210517(17)230516
B企业选择用生产日期+批号+序列号 来编制 PI,产品生产日期是 2021-5-17.批号是L243C4.序列号是 2153.那么PI就是:(11)210517(10)L243C5(21)2153
我们来看一下两个常见的 UDI-PI示例:
第一个PI选用了生产日期和序列号,可追溯到每个产品;

第二个PI选用了批号和到期日,对有效期的要求比较高。

接着是完整的 UDI 范例图:

包装识别符:0~9 的数字表示单个成品包装,用来区分同一款产品不同的包装层级,用得最多。
四、制作 UDI 一维、二维条码或 RFID 标签
接下来是第四步:根据指南生产 UDI 一维、二维条码或 RFID 标签。
我们先要确定打码方式,可以使用一种或者自由组合的方式,但要注意客户方是否有对应的扫码设备。
然后是打码设备的采购 来看下样图:

要注意检测条码是否正确哦!
GS1提供了免费检验条码的服务,您可以将您打印好的UDI条码寄给中国物品编码中心上海分中心进行测试。
五、UDI EUDAMED UDI数据库申报
欧盟udi的数据库录入是EUDAMED,但目前暂未开放。
UDI是什么?UDI长什么样子?能看下图片吗?如何读懂UDI码?怎么辨别UDI码正不正确?不少企业在刚接触UDI的时候,都会有这样的疑问。
而且即便是接触过UDI相关内容后,由于没有经历过实操,缺少关于UDI的直观印象,对UDI的认识仍然比较模糊。
那么UDI码到底长什么样子?呈现形式是什么?有没有完整版样品可以查看参考?今天UDI公共平台就以实际案例,为大家讲解UDI在实际应用中的展现。
UDI是什么
UDI是医疗器械唯一标识的缩写。

这是标准文件中对医疗器械唯一标识(UDI)给出的释义。
UDI虽然由数字、字母和符号的代码组成,但出现在产品上却是由标签作为载体承载,包括常用的条形码(一维码)和二维码。
完整的UDI码


一般来说,由于一维码包含内容越多条码越长,影响扫码,因此二维码的应用前景更广。
此外,MA编码结构和GS1编码结构均可生成二维码,不过MA标签载体一般采用QR码,GS1标签载体采用DM码生成。
UDI结构所含字符意义
医疗器械唯一标识包括产品标识和生产标识。产品标识为识别注册人/备案人、医疗器械型号规格和包装的唯一代码;生产标识由医疗器械生产过程相关信息的代码组成,根据监管和实际应用需求,可包含医疗器械序列号、生产批号、生产日期、失效日期等——《医疗器械唯一标识系统规则》第七条
以上示例的UDI码标签上的字符分别是UDI的两个组成部分,DI(产品标识)和PI(生产标识)。其中,DI位数固定,PI位数不定。
以MA编码结构为例

DI 由数字、字母和符号组成,包含发码机构代码、行业代码、制造商编码、包装编码、产品编码和校验位。
PI 一般包含生产日期、失效日期、生产批次以及序列号等内,具体内容根据企业实际情况而定。比如M代表生产日期,E代表失效日期,L代表生产批次,S代表序列号。
以GS1编码结构为例
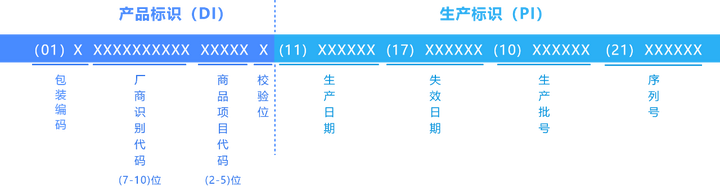
DI 由数字组成,包含包装编码、厂商识别代码、商品项目代码和校验位。
PI 应用标识符由数字指代。比如11代表生产日期,17代表失效日期,10代表生产批次,21代表序列号。